Autori:
Oana Otilia Niculiță
Universitatea de Medicină și Farmacie “Carol Davila”, București, România
Institutul Clinic Fundeni, Secția Clinică de Pediatrie, București, România
Cristina Georgiana Jercan
Universitatea de Medicină și Farmacie “Carol Davila”, București, România
Institutul Clinic Fundeni, Secția Clinică de Pediatrie, București, România
Anca Coliță
Universitatea de Medicină și Farmacie “Carol Davila”, București, România
Institutul Clinic Fundeni, Secția Clinică de Pediatrie, București, România
Introducere
Tumorile solide reprezintă 30% din toate cazurile de cancer la copii, exceptând tumorile cerebrale. Managementul tumorilor solide este complex și include: chimioterapie, intervenții chirurgicale, radioterapie și, în cazurile cu risc ridicat, transplant de celule stem (TCS). Mucozita orală (MO) este cea mai frecventă complicație la pacienții copii cărora li s-a efectuat TCS. La persoanele cărora li se face transplant, MO poate avea o evoluție pe termen lung, uneori severă.
Am analizat rezultatele pacienților copii cu tumori solide și tratați cu transplant de celule stem hematopoietice (TCSH) la Institutul Clinic Fundeni, între ianuarie 2002 și octombrie 2018 pentru a evalua durata medie a episodului de MO și a gradului de severitate conform numărului de proceduri efectuate.
Materiale și metode
Am analizat retrospectiv pacienții cu tumori solide și TCSH. Diagnosticele pacienților: neuroblastom (NBL), tumoră cu celule germinale, sarcom Ewing, nefroblastom. Pacienții au fost împărțiți în două grupuri: primul grup cu un singur TCSH și al doilea grup cu mai mult de un singur TCSH.
Criteriile utilizate pentru a evalua severitatea MO au fost, conform OMS: Gradul 1: sensibilitate ± eritem, Gradul 2: eritem, leziuni ulcerate, pacientul poate consuma alimente solide, Gradul 3: leziuni ulcerate cu eritem extins, pacientul nu poate înghiți alimente, Gradul 4: mucozită care nu permite alimentarea.
Toți pacienții au realizat măsuri profilactice de prevenire a MO: curățarea cavității bucale cu soluție de bicarbonat de sodiu, spălarea cavității bucale cu apă de gură pe bază de clorhexidină, spray oral cu Gel X. Toți pacienții au primit profilaxie antibiotică, antivirală și antifungică, nutriție parenterală și tratament suportiv.
Toți părinții au semnat formulare de consimțământ informat. Am efectuat analiza statistică utilizând testul chi pătrat.
Rezultate
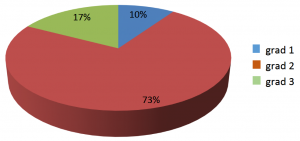
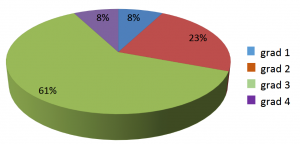
În clinica noastră, în perioada ianuarie 2002 – octombrie 2018, au fost efectuate 67 de proceduri de auto-TCSH la 52 de pacienți: 34 (65,3%) pacienți cu NBL, 9 (17,3%) pacienți cu sarcom Ewing, 6 (11,6%) pacienți cu tumoră cu celule germinale și 3 (5,8%) pacienți cu nefroblastom. Pacienții au fost împărțiți în două grupuri: primul grup cu o singură procedură TCS (79% din pacienți) și al doilea grup cu mai mult decât o singură procedură TCS (21% din pacienți). Pacienții au fost diagnosticați, stadializați și au primit tratament conform protocoalelor internaționale. Distribuția pe sexe a fost de 18 F/34 M. Distribuția pe vârste: 1-4 ani 38% (20 pacienți), 4-10 ani 35% (18 pacienți), > 10 ani 27% (14 pacienți). Distribuția pacienților conform gradului de MO este reprezentată în Figura 1.
Durata medie a MO în primul grup a fost de 6 zile (variație de la 3 la 17 zile), în vreme ce în al doilea grup a fost de 13 zile (variație de la 3 la 21 de zile). Pacienții din primul grup au primit analgezice pe o durată medie de 7 zile, în vreme ce pentru al doilea grup, perioada a fost prelungită la 13 zile. De asemenea, pentru cel de al doilea grup am observat că a crescut perioada de grefare, odată cu perioada de spitalizare și măsurile suportive. Pacienții cu multiple ședințe de chimioterapie și cu multiple spitalizări au prezentat risc crescut de infecție, iar pe durata celui de al doilea set de proceduri au dezvoltat diverse complicații infecțioase. Pacienții din ambele grupuri s-au vindecat total de MO până în momentul externării.
Un singur TCSH
Concluzie
Toți pacienții din studiul nostru au dezvoltat mucozită orală, deși au fost luate măsuri profilactice.
Nu au fost identificate corelații între gradul de severitate al MO și vârsta sau sexul pacientului.
Durata medie a episodului de MO este mai mare la pacienții cu TCS multiple (13 zile versus 6 zile).
Incidența unei MO severe după primul TCSH a fost de 17%, în vreme ce după TCSH în tandem a fost de 69% (P<0,0001).
Referințe
1. Carulli G, Rocco M, Panichi A, et al. Treatment of oral mucositis in hematologic patients undergoing autologous or allogeneic transplantation of peripheral blood stem cells: a prospective, randomized study with a mouthwash containing camelia sinensis leaf extract. Hematol Rep. 2013;5(1):21-5. Published 2013 Apr 4. doi:10.4081/hr.2013.e6
2. The Incidence and Severity of Oral Mucositis among Allogeneic Hematopoietic Stem Cell Transplantation Patients: A Systematic Review Chaudhry, Hafsa M. et al, Biology of Blood and Marrow Transplantation , Volume 22 , Issue 4 , 605 – 616
3. Staudenmaier, T., Cenzer, I., Crispin, A. et al. Support Care Cancer (2018) 26: 1577. https://doi.org/10.1007/s00520-017-4000-5
4. Gabriel, Don & Shea, Thomas & Olajida, Oludamilola & Serody, Jonathan & Comeau, Terrance. (2004). The Effect of Oral Mucositis on Morbidity and Mortality in Bone Marrow Transplant. Seminars in oncology. 30. 76-83. 10.1053/j.seminoncol.2003.11.040.
Contact
motilia24@yahoo.com
Oral mucositis in autologous stem cell transplantation for solid tumors in children: comparison between single and tandem procedures
Authors:
Oana Otilia Niculiță
1. „Carol Davila” University of Medicine and Pharmacy, Bucharest, Romania
2. Fundeni Clinical Institute, Pediatric BMT Dept., Bucharest, Romania
Cristina Georgiana Jercan
1. „Carol Davila” University of Medicine and Pharmacy, Bucharest, Romania
2. Fundeni Clinical Institute, Pediatric BMT Dept., Bucharest, Romania
Anca Coliță
1. „Carol Davila” University of Medicine and Pharmacy, Bucharest, Romania
2. Fundeni Clinical Institute, Pediatric BMT Dept., Bucharest, Romania
Background
Solid tumors represent 30% of all pediatric cancers, excepting brain tumors. The management of solid tumours is complex and includes chemotherapy, surgery, radiotherapy and, in high-risk cases, stem cell transplantation (SCT). Oral mucositis (OM) is the most frequent complication of pediatric patients undergoing SCT. In transplant recipients OM can have long-term evolution, sometimes severe.
We analyzed the results of pediatric patients with solid tumours and HSCT treated in Fundeni Clinical Institute between January 2002 and October 2018 to evaluate the median duration of OM episode and grade of severity according to the numbers of procedures performed.
Matherials and methods
We retrospectively analyzed patients with solid tumours and HSCT. Patients diagnosis: neuroblastoma (NBL), germ-cell tumour (GCT), Ewing sarcoma, nefroblastoma. Patients were divided into 2 groups: first group with one HSCT and second groupwith more than one HSCT.
Criteria used to asess severity of OM were, according to WHO: Grade 1 – soreness ± erythema, Grade 2 – erythema, ulcers; patient can swallow solid food, Grade 3 – ulcers with extensive erythema; patient cannot swallow food, Grade 4 – mucositis to the extent that alimentation is not possible.
All patients performed prophylactic measurements to prevent OM : mouth cleansing with sodium bicarbonate solution, mouthwash with clorhexidine, oral spray with Gel X. All patients received antibiotic, antiviral and antifungal prophylaxis, parenteral nutrition and supportive treatment.
All parents signed informed consent forms. We performed the statistical analysis using chi square test.
Results
In our clinic, between January 2002 and October 2018, were performed 67 auto-HSCT procedures to 52 patients: 34 (65.3%) pts with NBL, 9 (17.3%) pts with ES, 6 (11.6%) pts with GCT and 3 (5.8%) pts with nefroblastoma. Patients were divided into 2 groups: first group with a single SCT procedure (79% of pts) and second group with more than one SCT procedure (21% of pts). Patients were diagnosed, staged and received treatment according to international protocols. Sex ratio was 18F/34M. Age distribution:1-4 y 38% (20 pts), 4-10 y 35% (18 pts), > 10 y 27% (14 pts). Distribution of patients according to grade of OM is represented in Figure 1. The median duration of OM in the first group was 6 days (range 3 to 17 days), while in the second group was 13 days (range 3 to 21 days). For the first group patients received pain medication for an average of 7 days, whereas for the second group the period increased to 13 days. Also, for the second group we noticed the engraftment period increased, along with the hospitalization and supportive measures. Patients with multiple courses of chemotherapy and with multiple hospitalizations presented increased infectious risk and during the second procedures developed various infectious complications. Patients from both groups presented full recovery of oral mucositis by the time they were discharged.
Conclusion
All patients in our study have developed oral mucositis, though prohylaxis measurements have been used. We did not find corelations between the severity of OM and age or sex of patients.
The median duration of OM episode is increased in patients with multiple SCT (13 days versus 6 days) .
The incidence of severe OM after the first HSCT was 17%, whereas after tandem HSCT was 69% (P<0,0001).
References
1. Carulli G, Rocco M, Panichi A, et al. Treatment of oral mucositis in hematologic patients undergoing autologous or allogeneic transplantation of peripheral blood stem cells: a prospective, randomized study with a mouthwash containing camelia sinensis leaf extract. Hematol Rep. 2013;5(1):21-5. Published 2013 Apr 4. doi:10.4081/hr.2013.e6
2. The Incidence and Severity of Oral Mucositis among Allogeneic Hematopoietic Stem Cell Transplantation Patients: A Systematic Review Chaudhry, Hafsa M. et al, Biology of Blood and Marrow Transplantation , Volume 22 , Issue 4 , 605 – 616
3. Staudenmaier, T., Cenzer, I., Crispin, A. et al. Support Care Cancer (2018) 26: 1577. https://doi.org/10.1007/s00520-017-4000-5
4. Gabriel, Don & Shea, Thomas & Olajida, Oludamilola & Serody, Jonathan & Comeau, Terrance. (2004). The Effect of Oral Mucositis on Morbidity and Mortality in Bone Marrow Transplant. Seminars in oncology. 30. 76-83. 10.1053/j.seminoncol.2003.11.040.
Contact
motilia24@yahoo.com
Descarcare documente: